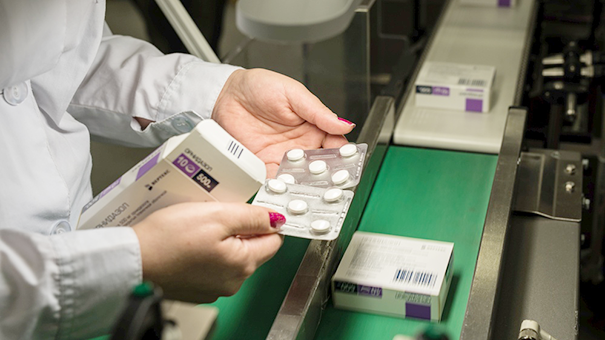
Маркировка ЛС станет лицензионным требованием для их производства
Министерство здравоохранения подготовило изменения в Положение о лицензировании производства лекарственных средств. Ведомство предлагает сделать участие в системе маркировки ЛС обязательным требованием для получения лицензии. Текст проекта опубликован 1 июля на портале проектов нормативных актов.
Минздрав предлагает добавить к обязательным требованиям, предъявляемым к лицензиату, наличие действующей регистрационной записи в системе мониторинга движения лекарственных препаратов, а также соблюдение требований о нанесении средств идентификации на упаковку ЛС. Актуальные требования к лицензиату описаны в Постановлении Правительства РФ от 6 июля 2012 г. № 686.
Ранее глава Росздравнадзора Михаил Мурашко заявил, что подключение к системе маркировки также станет лицензионным требованием и для аптек.
Напомним, что, согласно Постановлению Правительства № 1557, с 1 июля 2019 года субъекты обращения лекарственных средств, занимающиеся оборотом препаратов из перечня высокозатратных нозологий, должны будут зарегистрироваться в системе мониторинга движения ЛС и пройти необходимое тестирование на работоспособность установленных ими систем. С 1 октября нанесение маркировки на упаковку таких ЛС станет обязательным.
Ранее производители на совещании в Минпромторге рассказали, что внедрение маркировки повысит себестоимость производства лекарств.
2814 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль


зарегистрированным пользователям