Автор перевода: Александра Варшал
По материалам: Ventricular tachycardia — an atypical initial presentation of sarcoidosis: a case report
Meera Ekka, Sanjeev Sinha, Raghunandan Purushothaman, Nitish Naik, Rajiv Narang and Lavleen Singh,
Journal of Medical Case Reports 2013, 7: 196
Индианка, 41 год, поступила в стационар с приступами тахикардии, которые периодически повторялись на протяжении последних 10 дней. Она отрицала лихорадку, кашель, боль в грудной клетке, диспноэ, синкопальные состояния и другие симптомы, которые бы могли помочь в диагностике. Хронические заболевания (гипертонию, ИБС, сахарный диабет, заболевания щитовидной железы и системные болезни) пациентка также отрицала. В 1992 году больная прошла шестимесячный курс лечения по поводу туберкулеза легких. При осмотре пациентки температура тела в норме, пульс ритмичный 1–42 удара в минуту, АД — 120/70 мм рт. ст. На медиальной поверхности ног, над лодыжками, имелись коричневатые восковидные папулы. Других отклонений при осмотре не выявлено. В кардиологическом отделении пациентке с помощью электрокардио-версии успешно остановили желудочковую тахикардию (ЖТ).
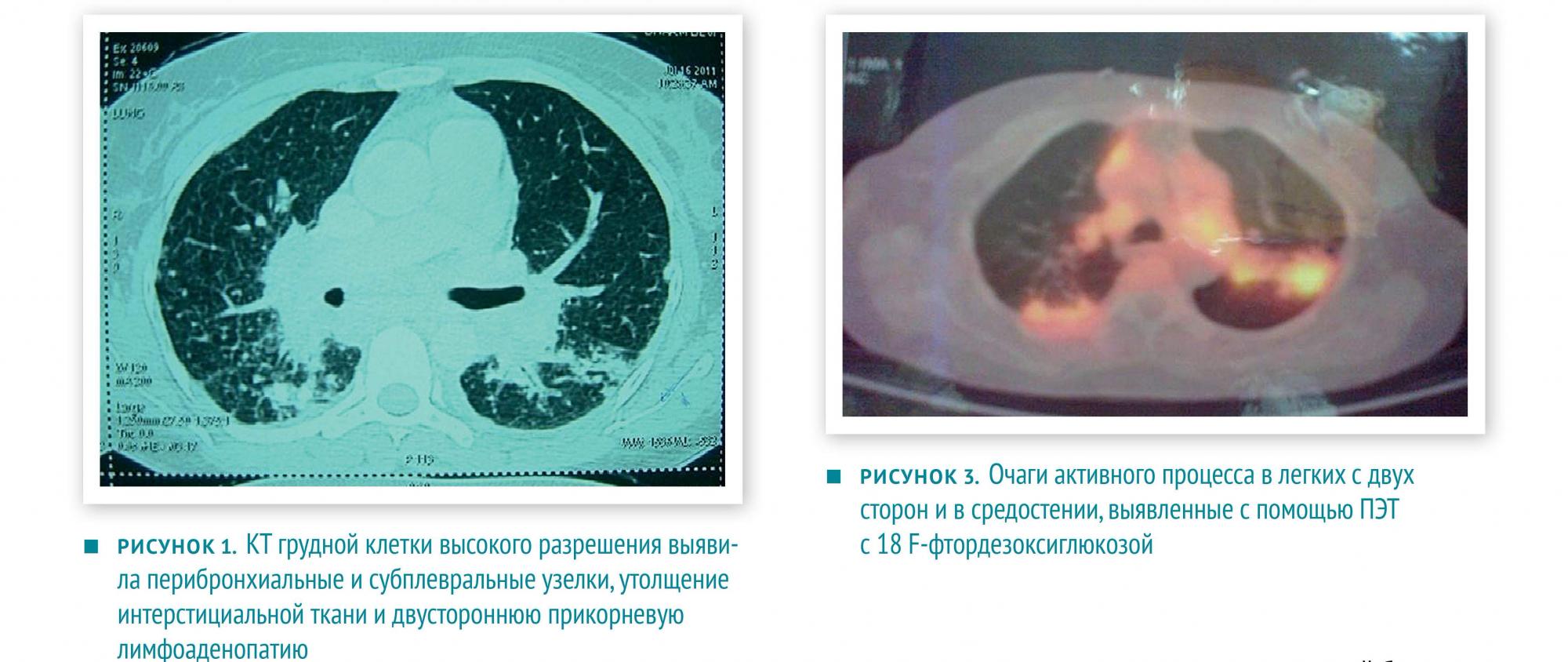
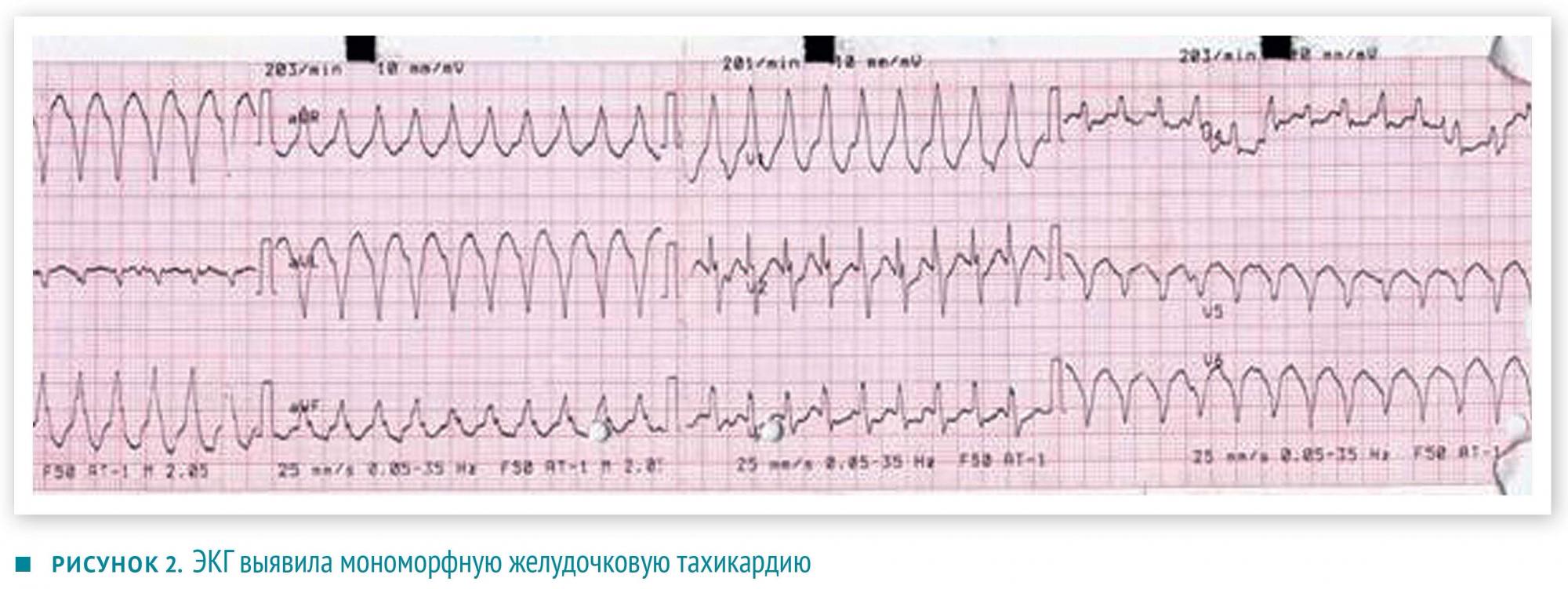
ОАК, биохимия крови, в том числе показатели, характеризующие функцию печени и почек, тиреоидные гормоны были в пределах нормы. Кальций в сыворотке крови, СОЭ — в пределах нормы, С-реактивный белок отрицательный. КТ грудной клетки с контрастированием выявила изменения, характерные для III стадии саркоидоза (рисунок 1). При ЭКГ зарегистрирована мономорфная ЖТ и блокада правой ножки пучка Гиса, электрическая ось сердца смещена вправо (рисунок 2).
Чтобы оценить стадию саркоидоза, врачи провели позитронно-эмиссионную томографию (ПЭТ)
с 18 F-фтордезоксиглюкозой. Результаты показали вовлеченность в патологический процесс обоих легких, средостения, лимфоузлов около поджелудочной железы и в правой надключичной области и фокальное поражение VII и VIII сегментов печени (рисунок 3). Надключичные лимфоузлы не пальпировались, поэтому биопсию взяли из поверхностного очага правой доли печени. Выявлен интерстициальный фиброз, эпителиоидные гранулемы не обнаружены.
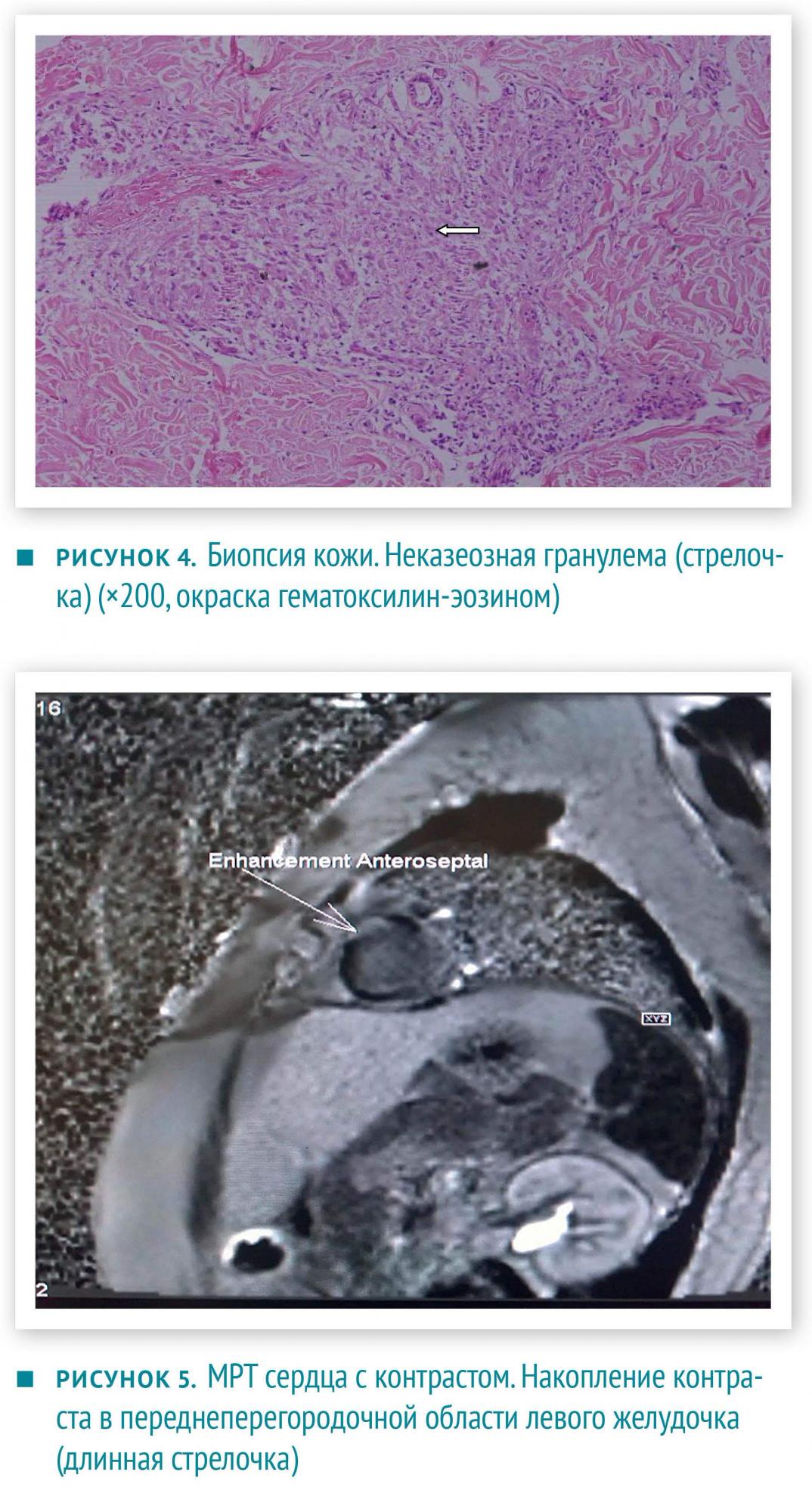
Тогда взяли на биопсию восковидную папулу с голени пациентки — обнаружена неказеозная эпителиоидная гранулема, похожая на саркоидную (рисунок 4). Окраска по Цилю-Нильсену микобактерий не выявила. Таким образом, диагностирован системный саркоидоз с поражением сердца.
Неказеозные эпителиоидные гранулемы (саркоидные гранулемы) — главный морфологический признак саркоидоза. Они состоят в основном из эпителиоидных клеток — больших мононуклеарных гистиоцитов, которые появляются при хроническом воспалении. Также встречаются лимфоидные клетки и полинуклеарные гигантские клетки Пирогова — Лангханса.
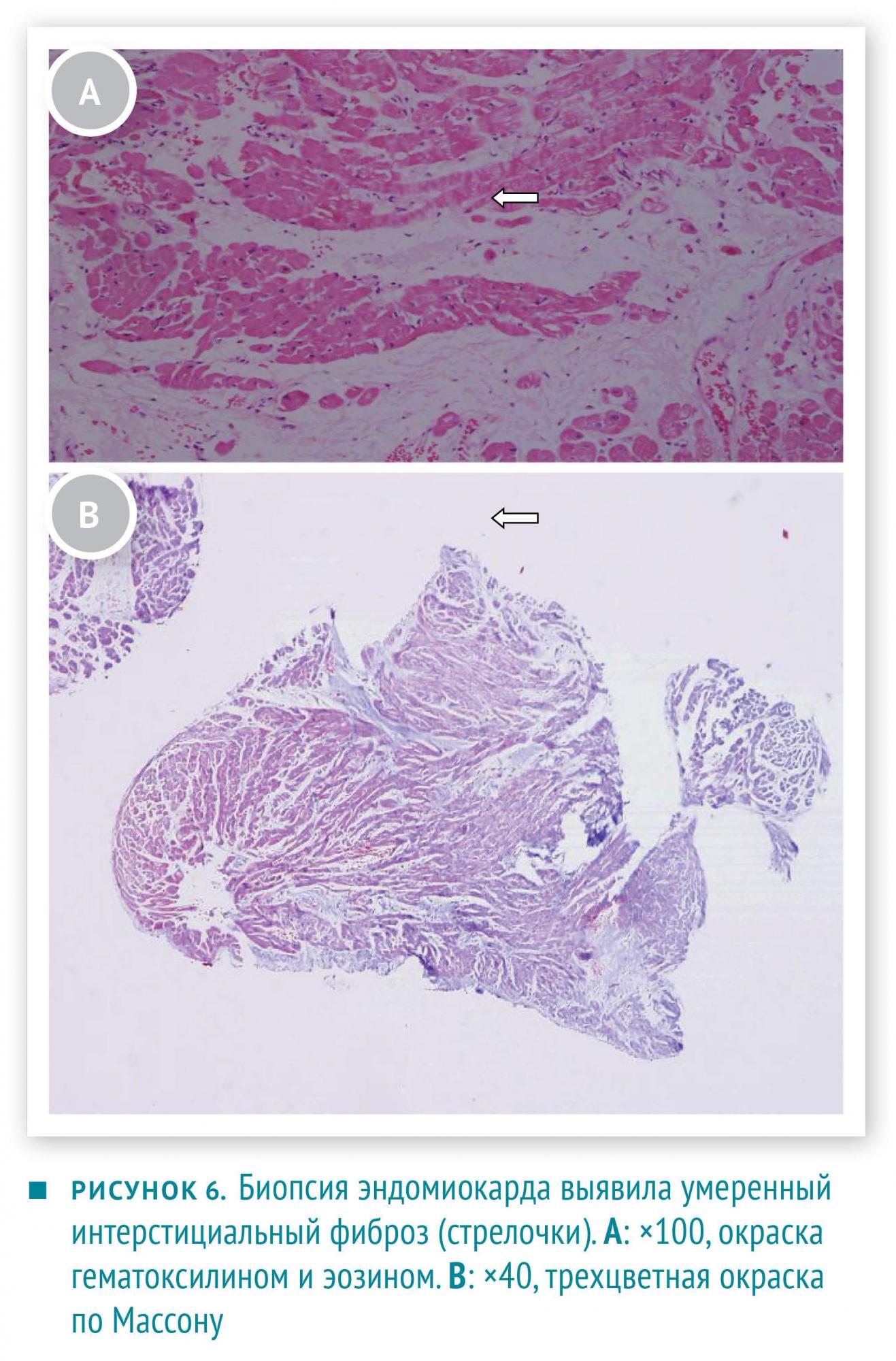
Холтеровское мониторирование зафиксировало длительные эпизоды мономорфной ЖТ. При коронарной ангиографии отклонений обнаружено не было. При эхокардиографии установлено: фракция выброса (ФВ) левого желудочка — 48 %, имеется гипокинезия средне-нижней части межжелудочковой перегородки. МРТ с гадолиниевым контрастированием выявила характерное для фиброза запоздалое поглощение контраста в апикальной и переднеперегородочной части левого желудочка (рисунок 5). Далее больная подверглась эндомиокардиальной биопсии с целью уточнения патологического процесса в сердце. Были обнаружены очаги интерстициального фиброза, гранулем не обнаружено (рисунок 6A, 6B).
Клинически и лабораторные данные соответствовали диагностическим критериям системного саркоидоза с поражением сердца [5]. Кроме симптоматической терапии ей был назначен преднизолон в дозировке 1 мг/кг/день. Антиаритмики (амиодарон per os 300 мг в день и метопролол 100 мг два раза в день) не купировали ЖТ. Дважды проводили радиочастотную абляцию сердца, однако операции не помогли купировать ЖТ.
На имплантацию кардиовертера-дефибриллятора у пациентки не было средств. Через неделю пациентка скончалась в стационаре от приступа фибрилляции желудочков, которая не купировалась дефибрилляцией. Родственники пациентки отказались от аутопсии.
Обсуждение
Саркоидоз — это мультисистемное гранулематозное заболевание неизвестной этиологии, которое поражает в основном легкие, кожу, глаза и лимфатическую систему. Подвержены саркоидозу в основном молодые люди 20–30‑лет обоих полов. У большинства пациентов в патологический процесс вовлечена легочная ткань. Кроме легких часто поражаются кожа, ЖКТ, глаза, нервная система (приведены в порядке убывания частоты поражения) [6]. Симптомы поражения сердца встречаются редко — в 2–5 % случаях саркоидоза [1, 2], и реже других симптомов являются манифестными. Тем не менее поражение сердечной мышцы может течь асимптоматично и выявляться лишь при аутопсии. У 20–25 % больных саркоидозом при аутопсии находят характерные изменения в сердечной мышце. Поражение сердца может проявиться сердечной недостаточностью, атриовентрикулярной блокадой сердца, желудочковой аритмией или внезапной смертью [6, 8].
Незначительные смазанные симптомы поражения сердца вскоре могут обернуться летальным исходом [3]. Поэтому важны ранняя диагностика и лечение кардиального саркоидоза, которые помогут снизить риск внезапной сердечной смерти [4]. Выше представлен редкий случай, когда у пациентки саркоидоз манифестировал сердечной симптоматикой и закончился летально.
Течение саркоидоза медленное, но острые осложнения со стороны сердца могут повлечь летальный исход [9, 10]. Эпителиоидные гранулемы миокарда нарушают проведение электрического импульса в миокарде, возникает механизм re-entry, который провоцирует желудочковую тахикардию [11].
Прижизненная диагностика кардиального саркоидоза сложна, поскольку требуются высокотехнологичные и инвазивные методы исследования [5, 12]. Вероятность обнаружения эпителиоидных гранулем при эндомиокардиальной биопсии всего лишь около 20 % [15].
Поражение сердца при саркоидозе требует неотложного назначения
глюкокортикостероидов, возможно, в комбинации с другими иммуносупрессантами [16]. В недавнем исследовании было показано, что эффективность кортикостероидов выше при сохранности ФВ левого желудочка на уровне 30–50 %, при тяжелом поражении миокарда, когда ФВ менее 30 %, терапия не улучшает состояния, возможно, из‑за необратимости поражения миокарда [17]. В описанном случае у пациентки было тяжелое поражение миокарда и она не отвечала на терапию стероидами.
Диагностика кардиального саркоидоза — критерии министерства здравоохранения, труда и социального благополучия Японии
Если характерные гранулемы при эндомиокардиальной биопсии не обнаружены, то для установки диагноза необходимо наличие двух и более больших критериев или одного большого критерия и как минимум двух малых.
Большие критерии
- Атривентрикулярная блокада высокой степени
- Базальное истончение межжелудочковой
- перегородки
- Повышенное накопление галлия-67 в сердце (при сцинтиграфии)
- Понижение ФВ левого желудочка (<50 %)
Малые критерии
- Аномалии при ЭКГ: желудочковые аритмии (тахикардия, мультифокальное или преждевременное сокращение желудочков), полная блокада правой ножки пучка Гиса, отклонение электрической оси или ненормальная Q волна
- Аномалии при эхокардиографии: локальное нарушение динамики миокарда или анатомический дефект (желудочковая аневризма, истончение стенки)
- Сцинтиграфия миокарда: дефекты наполнения таллием-201 или технецием-99m
- МРТ с гадолиниевым усилением: отсроченное накопление контраста в миокарде
- Эндомиокардиальная биопсия: интерстициальный фиброз или умеренная моноцитарная инфильтрация
Желудочковые аритмии часто встречаются при саркоидозе сердца, и часто рефрактерны к терапии антиаритмиками, в частности к амиодарону. Кардиохирурги рекомендуют имплантацию водителя ритма при полной блокаде атриовентрикулярной проводимости и имплантацию кардиовертера-дефибриллятора при фибрилляции желудочков или тахикардии и сниженной ФВ левого желудочка [18]. Трансплантация сердца — один из вариантов терапии кардиального саркоидоза, рефрактерного к лечению, однако ряд исследований указывает на повышенный уровень смертности в таких случаях [19, 20]. Тем не менее прогресс в терапии желудочковых аритмий привел к тому, что причиной смерти у пациентов с поражением сердца стали не нарушения ритма, а застойная сердечная недостаточность.
Заключение
Поражение сердца должно быть исключено у любого пациента с саркоидозом. Негативный результат эндомиокардиальной биопсии не исключает саркоидоз сердца, особенно если есть другие кардиальные симптомы. Стероидная терапия эффективна на ранних стадиях болезни. Высокая вероятность аритмий у таких пациентов ставит вопрос о профилактической имплантации кардиовертера-дефибриллятора.
Родственники пациентки дали письменное согласие на публикацию случая. Копия письменного согласия находится у главного редактора журнала (JOURNAL OF MEDICAL CASE REPORTS).
Baughman RP et al.: Clinical characteristics of patients in a case control study of sarcoidosis. Am J Respir Crit Care Med 2001, 164:1885–1889.
Dubrey SW, Bell A, Mittal TK: Sarcoid heart disease. Postgrad Med J 2007, 83:618–623.
Mori M, Hanon S, Rachko M: Case report: cardiac sarcoidosis presenting with ventricular arrhythmias: case report and review of the literature. Int J Cardiol 2007, 120: e21 — e23.
Habersberger J, Manins V, Taylor AJ: Cardiac sarcoidosis. Intern Med J 2008, 38:270–277.
Soejima K, Yada H: The work-up and management of patients with apparent or subclinical cardiac sarcoidosis: with emphasis on the associated heart rhythm abnormalities. J Cardiovasc Electrophysiol 2009, 20:578–583.
Iannuzzi MC, Rybicki BA, Teirstein AS: Sarcoidosis. N Engl J Med 2007, 357:2153–2165.
Tavora F et al.: Comparison of necropsy findings in patients with sarcoidosis dying suddenly from cardiac sarcoidosis versus dying suddenly from other causes. Am J Cardiol 2009, 104:571–577.
Brown ML et al.: Intraoperative diagnosis of isolated cardiac sarcoid. Heart Lung Circ 2007, 16:315–317.
Dubrey SW, Falk RH: Diagnosis and management of cardiac sarcoidosis. Prog Cardiovasc Dis 2010, 52:336–346.
Bargout R, Kelly RF: Sarcoid heart disease: clinical course and treatment. Int J Cardiol 2004, 97:173–182.
Furushma H et al.: Ventricular tachyarrhythmia associated with cardiac sarcoidosis: its mechanisms and outcome. Clin Cardiol 2004, 27:217–222
Hiraga H, Yuwai K, Hiroe M: Guideline for Diagnosis of Cardiac Sarcoidosis: Study Report on Diffuse Pulmonary Diseases from the Japanese Ministry of Health and Welfare. Tokyo: The Japanese Ministry of Health and Welfare; 1993:23–24.
Sharma S: Cardiac imaging in myocardial sarcoidosis and other cardiomyopathies. Curr Opin Pulm Med 2009, 15:507–512.
Youssef G et al.: Cardiac sarcoidosis: applications of imaging in diagnosis and directing treatment. Heart 2011, 97:2078–2087.
Uemura A, Morimoto S, Hiramitsu S, Kato Y, Ito T, Hishida H: Histologic diagnostic rate of cardiac sarcoidosis: evaluation of endomyocardial biopsies. Am Heart J 1999, 138:299–302.
Chapelon-Abric C et al.: Cardiac sarcoidosis: a retrospective study of 41 cases. Med Baltim 2004, 83:315–334.
Chiu CZ et al.: Prevention of left ventricular remodeling by long-term corticosteroid therapy in patients with cardiac sarcoidosis. Am J Cardiol 2005, 95:143–146.
Grimm W, Alter P, Maisch B: Arrhythmia risk stratification with regard to prophylactic implantable defibrillator therapy in patients with dilated cardiomyopathy. Results of MACAS, DEFINITE, and SCD-HeFT. Herz 2004, 29:348–352.
Chang TI et al.: Isolated cardiac sarcoidosis in heart transplantation. Transpl Proc 2012, 44:903–906.
Akashi H et al.: Outcome of patients with cardiac sarcoidosis undergoing cardiac transplantation — single-center retrospective analysis. J Cardiol 2012, 60:407–410.



 Катрен Стиль
Катрен Стиль
зарегистрированным пользователям