
Ревматоидный артрит: в фокусе — клинические рекомендации
Предпосылки, причины, последствия и стандарты лечения ревматоидного артрита
Ревматоидный артрит считается одной из самых тяжёлых иммуновоспалительных патологий. Перед вами — краткий обзор актуальных клинических рекомендаций, в которых отражена основная информация о причинах, патогенезе, диагностике и фармакотерапии ревматоидного артрита.
От определения к проявлениям
Фармспециалисту важно помнить, что ревматоидный артрит (РА) представляет собой аутоиммунное ревматическое заболевание, которое характеризуется прогрессирующей деструкцией суставов и поражением внутренних органов. Уже в течение 3–5 лет после манифестации РА вызывает стойкую потерю трудоспособности у половины пациентов, при этом следует учитывать, что пик заболеваемости приходится на наиболее трудоспособный возраст 40–55 лет.
При отсутствии эффективной терапии продолжительность жизни у пациентов с РА на 10 лет меньше, чем людей, не страдающих этим заболеванием, в первую очередь за счет высокого риска развития коморбидных заболеваний: сердечно-сосудистых, остеопороза, тяжелых инфекций, онкологических.
Этиология РА неизвестна. Однако очевидно, что риск развития заболевания повышается при воздействии широкого спектра факторов: генетических, гормональных, факторов окружающей среды (загрязнение воздуха, курение, инфекция), метаболических (дефицит витамина D, ожирение и другие). Суть патологического процесса составляет системное аутоиммунное воспаление, которое быстро затрагивает синовиальную оболочку суставов. Более чем у 90 % пациентов обнаруживаются широкий спектр аутоантител в крови, наиболее характерные — ревматоидные факторы.
Примерно в половине случаев заболевание начинается с постепенного, в течение месяцев нарастания болей и скованности преимущественно в мелких суставах кистей и стоп. Обычно в начале клинические проявления выражены умеренно и часто носят субъективный характер. Но иногда болезнь дебютирует как острый артрит крупных суставов.
Пациентов могут тревожить:
- утренняя скованность, длительность не менее 30–60 минут (в отличие от остеоартроза, там скованность разрешается гораздо быстрее);
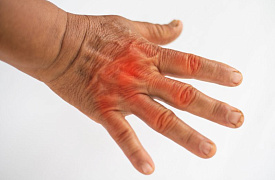
- припухлость суставов, локальная гипертермия кожи;
- болезненность суставов при пальпации и движении;
- уменьшение объёма активных и пассивных движений в суставах;
- появление деформаций суставов;
- невозможность сжать кисть в кулак — характерный признак РА — и т. д.
Фармакотерапия ревматоидного артрита
Цель лечения РА — достижение ремиссии или низкой активности заболевания. У пациентов, находящихся в ремиссии, трудоспособность и прогноз лучше, чем у больных в активной стадии заболевания.
НПВП и парацетамол рекомендуются для уменьшения болей в суставах. Практически все НПВП могут уменьшать боль при назначении в дозах, значительно меньших, чем те, что требуются для подавления воспаления.
При умеренной вероятности развития осложнений со стороны ЖКТ назначают селективные НПВП без дополнительной профилактики или неселективные НПВП на фоне ингибиторов протонной помпы. При недостаточной эффективности или наличии противопоказаний к назначению НПВП и парацетамола для уменьшения болей рекомендуется назначать комбинацию трамадол + парацетамол в течение срока, не превышающего 2 недели.
Синтетические базовые противовоспалительные препараты (сБПВП) — аналоги фолиевой кислоты, кишечные противовоспалительные препараты аминосалициловая кислота и аналогичные, селективные иммунодепрессанты, противомалярийные средства. Рекомендуется назначать сБПВП всем пациентам с РА, в том числе пациентам с высокой вероятностью развития РА с момента постановки диагноза. Если через три месяца терапии удалось достичь умеренного эффекта, терапию рекомендуется продолжить в течение следующих 3 месяцев.
Метотрексат рекомендуется всем пациентам с ревматоидным артритом как препарат первой линии лечения, а также пациентам с недифференцированным артритом при высокой степени развития РА.
- Препарат назначают индивидуализировано в зависимости от активности заболевания и риска развития нежелательных лекарственных реакций.
- Метотрексат не рекомендуется назначать беременным или планирующим беременность женщинам в связи с высоким риском побочных эффектов для матери и ребёнка.
- На фоне лечения метотрексатом рекомендуется приём фолиевой кислоты не менее 5 мг в неделю. Ёе назначают не ранее, чем через 24 часа после перорального приёма или парентерального введения метотрексата.
При наличии противопоказаний для назначения метотрексата или плохой его переносимости рекомендуется назначить лефлуномид или сульфасалазин.
Гидроксихлорохин может быть рекомендован в качестве монотерапии у пациенток во время беременности в случае низкой активности заболевания.
Глюкокортикостероиды при РА назначают только врачи-ревматологи. Лечение проводят в комбинации с метотрексатом (или другими сБПВП) в течение времени, необходимого для развития эффекта, и коротким курсом при обострении на любой стадии РА. Назначение глюкокортикостероидов проводят с учётом высокого риска побочных эффектов — развития иммунодефицита, эрозивно-язвенных заболеваний ЖКТ, серьёзных заболеваний сердечно-сосудистой системы, дислипидемии, сахарного диабета, системного остеопороза и других. У всех пациентов, получающих глюкокортикостероиды более трёх месяцев в дозе более 5 мг в день, рекомендуется проводить профилактику остеопороза с помощью препаратов кальция в комбинации с витамином D и, при необходимости, лечение глюкокортикоидного остеопороза (бисфосфонаты, в том числе алендроновая кислота, ибандроновая кислота, ризедроновая кислота, золедроновая кислота).
Генно-инженерные биологические препараты (ингибиторы фактора некроза опухоли альфа, ингибиторы интерлейкина, моноклональные антитела, селективные иммунодепрессанты) или таргетные сБПВП (селективные иммунодепрессанты барицитиниб, тофацитиниб, упадацитиниб) рекомендуются при отсутствии противопоказаний пациентам с факторами риска неблагоприятного прогноза. Лечение рекомендуется проводить в комбинации с метотрексатом для увеличения эффективности терапии. Возможна комбинация с другими сБПВП.
Антифибротическая терапия (нинтеданиб и другие) рекомендуется пациентам с РА и интерстициальным заболеванием лёгких для замедления прогрессирующего снижения лёгочной функции, снижения риска обострений и увеличения продолжительности жизни.
Особые случаи
- При недостаточной эффективности монотерапии метотрексатом и отсутствии противопоказаний и факторов неблагоприятного прогноза рекомендовано переключение на монотерапию сульфасалазином или лефлуномидом или назначение комбинированной терапии метотрексат + сульфасалазин + гидроксихлорохин.
- При наличии противопоказаний для назначения и плохой переносимости метотрексата и других сБПВП рекомендовано проведение монотерапии генно-инженерными биологическими препаратами, в первую очередь ингибиторами интерлейкина (тоцилизумабом, сарилумабом, олокизумабом, левилимабом) или таргетными сБПВП (селективные иммунодепрессанты барицитиниб, тофацитиниб, упацитиниб).
- При отсутствии улучшения через 3 месяца или не достижении ремиссии/низкой активности РА через 6 месяцев от начала терапии генно-инженерными биологическими препаратами или таргетными сБПВП рекомендуется «переключить» пациента на лечение генно-инженерными биологическими препаратами с другим механизмом действия.
- При достижении ремиссии длительностью не менее 12 месяцев на фоне терапии, после отмены глюкокортикостероидов, рекомендуется контролируемое постепенное снижение («титрование») дозы или в редких случаях отмена генно-инженерных биологических препаратов. Для поддержания ремиссии после снижения или отмены препаратов необходима адекватная терапия метотрексатом, включая применение его подкожной формы.
- При достижении длительной стойкой ремиссии не менее 12 месяцев после прекращения лечения генно-инженерными биологическими препаратами рекомендуется рассмотреть возможность снижения дозы сБПВП по согласованию с пациентом.
Применение биоаналогов генно-инженерных биологических препаратов
Выбор оригинального генно-инженерного биологического препарата или его биоаналога рекомендуется проводить с учётом мнения квалифицированного врача-ревматолога и принципов доказательной медицины (доказанная терапевтическая эффективность и безопасность биоаналога).
Необходимо учитывать, что эффективность и безопасность биоаналогов при разных заболеваниях может отличатся от оригинальных ГИБП.
Оригинальный ГИБП не может автоматически заменяться на его биоаналог, замену проводят только на основе консенсуса врач-ревматолог-пациент.
8 апреля 2025
Текст: Мария Тропинина
Фото: www.istockphoto.com/Dobrila Vignjevic
Выпуск: №256, апрель 2025624 просмотров
624 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль.png)

зарегистрированным пользователям