
Убираем в карантин: обзор писем Росздравнадзора
Перечень лекарственных средств, отозванных из оборота в марте 2023 года
В прошедшем марте по решению производителей из гражданского оборота было отозвано 14 серий лекарственных препаратов. Обращение ещё 6 серий было прекращено Росздравнадзором из‑за обнаруженных несоответствий отобранных образцов требованиям нормативной документации. Удивительно, но в течение месяца Минздрав не опубликовал ни одного заявления производителей о прекращении государственной регистрации какого‑либо торгового наименования ЛС. Мы собрали все важные официальные данные из информационных писем Росздравнадзора в одной статье: списки отозванных препаратов, причины отзыва и краткие инструкции, как действовать в случае обнаружения их в ассортименте аптеки.
Отзыв
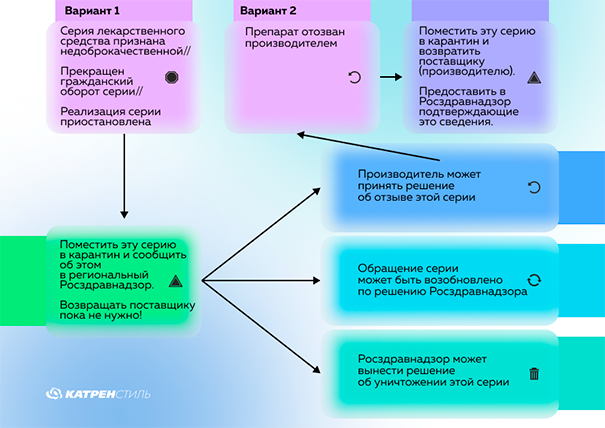
Отзыв препаратов происходит по инициативе производителя или его представителя (в случае с импортными ЛС), а Росздравнадзор информирует об этом всех участников процесса обращения ЛС и рекомендует им, как поступить. Рекомендации при отзыве ЛП стандартные:
Что делать производителю?
Предоставить в Росздравнадзор сведения об изъятии из обращения указанной серии лекарственного препарата.
Что делать аптекам и другим субъектам обращения ЛС?
Предоставить в территориальный орган Росздравнадзора сведения, подтверждающие возврат указанной серии лекарственного препарата поставщикам (производителю).
Мы объединили отзываемые препараты в одной таблице. В качестве причины в письмах Росздравнадзора зачастую указано «несоответствие качества препарата требованиям нормативной документации» по тому или иному показателю.
Таблица 1. Отозванные препараты
| Препарат | Серия | Производитель | Несоответствие показателю |
| «Цефазолин-АКОС, порошок для приготовления раствора для внутривенного и внутримышечного введения 1 г, флаконы (50), коробки картонные «Для стационаров»» | 250221 | ОАО «Синтез» (Россия) | «Аномальная токсичность» |
| «Магния сульфат, раствор для внутривенного введения, 250 мг/мл, 10 мл, ампулы (10), пачки картонные» | 511022 | ООО «Славянская аптека» (Россия) | «pH» |
| «Викасол, раствор для внутримышечного введения, 10 мг/мл, 1 мл, ампулы (10), пачки картонные» | 40721 | ПАО «Биосинтез» | В растворе присутствуют посторонние включения |
| «Цитрамон-ЛекТ, таблетки 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 851121 | ОАО «Тюменский химико-фармацевтический завод» (Россия) | «Распадаемость» |
| «Эналаприл, таблетки 10 мг 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 1150922, 1151121, 890622 | ПАО «Биосинтез» | «Родственные примеси» |
| «Эналаприл, таблетки 5 мг 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 130222, 951022, 470522 | ПАО «Биосинтез» | «Родственные примеси» |
| «Аторвастатин, таблетки, покрытые плёночной оболочкой, 10 мг 10 шт., упаковки ячейковые контурные (3), пачки картонные» | 101220 | ООО «Изварино Фарма» | В упаковках обнаружена инструкция по применению другого ЛС |
| «Ацетилсалициловая кислота-УБФ, таблетки 500 мг 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 70122 | ОАО «Уралбиофарм» (Россия) | «Растворение» |
| «Сульзонцеф, порошок для приготовления раствора для внутривенного внутримышечного введения 1500 мг + 1500 мг, флаконы (1), пачки картонные» | 150521 | ОАО «Синтез» (Россия) | Во флаконе обнаружен осколок стекла |
| «Натрия хлорид, растворитель для приготовления лекарственных форм для инъекций 0,9 % 10 мл, ампулы (10), пачки картонные» | 190722 | ФКП «Армавирская биофабрика» (Россия) | Неправильно указанный срок годности на стикере для КИЗ маркировки |
Прекращение обращения
Следующая группа — это ЛС, оборот которых прекращён по инициативе Росздравнадзора после обнаружения в ходе проверок несоответствия серий препаратов нормативным требованиям.
Что делать аптекам?
Провести проверку наличия указанных серий лекарственных препаратов и, в случае обнаружения таких ЛС, поместить их в карантин. О результатах проверки нужно проинформировать территориальные органы Росздравнадзора.
Таблица 2. Лекарственные средства, оборот которых приостановлен Росздравнадзором
| Препарат | Серия | Производитель | Несоответствие показателю |
| «Викасол, раствор для внутримышечного введения, 10 мг/мл, 1 мл, ампулы (10), пачки картонные» | 20320 | ПАО «Биосинтез» | В растворе присутствуют посторонние включения |
| «Цефтриаксон, порошок для приготовления раствора для внутривенного и внутримышечного введения 1 г, флаконы (1), пачки картонные» | 1541021 | ООО «Компания ДЕКО» (Россия) | «Стерильность» |
| «Гепазолон, суппозитории ректальные 120 ME + 10 мг + 1.7 мг 5 шт., упаковки ячейковые контурные (2), пачки картонные» | 27102022 | ООО «Альтфарм» (Россия) | «Описание» (суппозитории деформированы, с полостями на поверхности) |
| «Клиндамицин Дж, раствор для внутривенного и внутримышечного введения 150 мг/мл 4 мл, флаконы (5), пачки картонные» | JD3133 | «Джодас Экспоим Пвт. Лтд.» (Индия) | «Описание», «Прозрачность», «Механические включения» |
| «Амлодипин, таблетки 10 мг, 10 шт, упаковки ячейковые контурные (6), пачки картонные» | 20321 | ОАО «Марбиофарм» (Россия) | «Родственные примеси» |
| «Эналаприл, таблетки 5 мг 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 470522 | ПАО «Биосинтез» | «Родственные примеси» |
Следите за оперативными сообщениями о прекращении импорта или производства лекарственных препаратов (и об изменениях в инструкциях и новых данных по безопасности применения ЛС) в разделе «Новости», а также не пропускайте наш следующий ежемесячный обзор с перечислением всех изъятых и отозванных из обращения серий ЛС.
3 апреля 2023
Текст: Роман Сапрыкин
Фото: © Kzenon / Фотобанк Фотодженика
Выпуск: №232, апрель 20234563 просмотров
4563 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль


зарегистрированным пользователям