
Давление не падает
Фармакотерапия резистентной артериальной гипертонии (АГ) — единственная тактика с доказанной эффективностью
Лечение резистентной артериальной гипертензии (РАГ) является сложной фармакологической задачей, над которой работают учёные по всему миру. Так, группа российских авторов (Шепелева Н. Е., Родионов А. В., Фомин В. В.) провела анализ медицинской литературы по данному вопросу и предложила варианты персонифицированного подхода в фармакотерапии РАГ. Результаты их исследования были опубликованы в журнале «Терапевтический архив» под названием «Фармакотерапия резистентной артериальной гипертонии». Проведём краткий обзор этой публикации — надеемся, изложенные в ней данные помогут нашим читателям актуализировать уровень своих профессиональных знаний.
Актуальность вопроса
Как отмечают авторы исследования, в распоряжении современного врача находится широкий выбор антигипертензивных ЛС, а также различные схемы комбинированной терапии АГ. Несмотря на это, существует определённая доля пациентов (10–15 %), у которых не удаётся достичь целевых значений АД.
Анализ патогенеза резистентной формы АГ и поиск путей к решению этой проблемы является одной из важнейших задач клинической кардиологии [1]. При РАГ одновременное назначение трёх и более антигипертензивных ЛС в адекватных дозах, включая диуретик, не приводит к нормализации артериального давления.
Пациенты с РАГ больше подвержены сердечно-сосудистым осложнениям (инфаркт, инсульт, СН, хроническая болезнь почек (ХБП)), чем пациенты, у которых удалось достичь целевого уровня АД [2–7].
Причинами РАГ являются выбор врачом неоптимального режима терапии и назначение нерациональной комбинации ЛС, а также низкая приверженность пациента к лечению [8]. В то же время проведение рациональной комбинированной терапии не гарантирует, что РАГ не разовьётся.
Основные принципы комбинированной фармакотерапии артериальной гипертензии
Согласно рекомендациям Европейского общества кардиологов, базовая фармакотерапия АГ основана на назначении 5 основных групп ЛС:
- Блокаторы рецепторов к ангиотензину (БРА).
- Ингибиторы ангиотензин-превращающего фермента (ИАПФ).
- Антагонисты кальция (АК).
- Бета-адреноблокаторы (БАБ).
- Тиазидные диуретики (ТД).
Выбор ЛС зависит от преобладающих факторов риска, поражения органов-мишеней, сопутствующей патологии. При неэффективности ЛС первой линии назначают препараты второй линии: антагонисты минералокортикоидных рецепторов (АМР), амилорид или aльфа-адреноблокаторы [9].
Согласно британским клиническим рекомендациям NICE в качестве препаратов первой линии предлагается применять ИАПФ/БРА (у пациентов до 55 лет) или АК (55 лет и старше), затем их сочетание с дальнейшим добавлением ТД, БАБ, aльфа-адреноблокатора и АМР препараты [10].
Американские эксперты АНА/АСС также рекомендуют для повышения эффективности антигипертензивной терапии применять БАБ или АМР [11]. Ключевые моменты рекомендаций по лечению АГ представлены ниже.
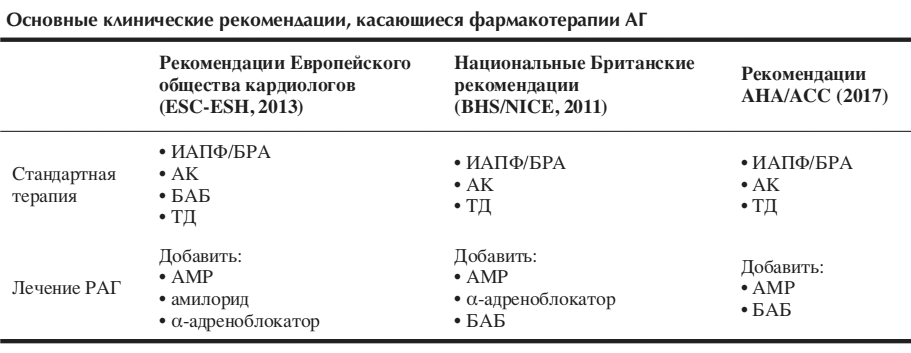
Несмотря на разные подходы к лечению АГ, принятые в разных странах, наблюдается сходство общих принципов терапии этого заболевания:
- в качестве препаратов первой линии назначают ИАПФ, БРА, АК и ТД;
- при неэффективности комбинации этих ЛС добавляют АМР, aльфа-адреноблокаторы и БАБ.
Также существуют рекомендации по замене тиазидных диуретиков на низкие дозы петлевых диуретиков (торасемид) [12]. Помимо этого, возможно назначение ЛС центрального действия из группы агонистов имидазолиновых рецепторов [13].
Исследования различных схем лечения АГ
Как отмечают авторы работы, у пациентов, получающих стандартную трехкомпонентную схему лечения, выбор четвёртого и пятого ЛС осуществляется эмпирически, так как нет чётких предикторов эффективности терапии.
Тем не менее некоторые авторы предприняли попытки создания алгоритмов лечения РАГ на основании учёта патогенеза развития АГ и анализа существующих клинических исследований.
С. Талер и соавторы [14] рекомендуют применять «гемодинамический подход» в терапии АГ. В проведённом ими исследовании все пациенты были разделены на 2 группы:
-
Коррекция лечения АГ проводилась с учётом показателей гемодинамики: периферического сосудистого сопротивления (ПСС), сердечного выброса (СВ), ортостатического измерения внутригрудного объёма крови (ВГОК).
Если СВ был ниже нормы, а ПСС выше нормы, то к терапии добавляли дигидропиридиновые антагонисты кальция, ИАПФ, БРА или прямой вазодилататор (гидралазин) или повышали их дозировку, снижая при этом дозу БАБ. При отсутствии изменения ВГОК при ортостазе — добавляли диуретик или повышали его дозировку.
При высоком СВ и низком ПСС в лечении добавляли БАБ или ЛС центрального действия, а также снижали дозу вазодилататоров. При отсутствии изменения ВГОК при ортостазе — добавляли диуретик или повышали его дозировку.
При нормальных значениях СВ и ПСС коррекцию лечения проводили за счёт назначения диуретиков.
- Коррекция терапии АГ проводилась эмпирически.
После 3 месяцев наблюдения в 1 группе целевого значения АД достигло 56 % пациентов, во 2 — всего 33 %. В 1 группе чаще назначали БАБ и прямые вазодилататоры, а во 2 — aльфа-адреноблокаторы и БАБ [14].
S. Hirsch и соавторы предложили простой алгоритм коррекции лечения АГ [15]. Выбор препаратов осуществлялся на основании физикальных данных и доступных для измерения показателей гемодинамики.
Пациентам с ЧСС более 84 уд./мин (активация симпатического отдела нервной системы) дополнительно назначали БАБ и АК недигидропиридинового ряда (верапамил, дилтиазем). При наличии периферических отёков и других признаков задержки жидкости в организме назначали диуретик.
При сочетании тахикардии с отёками назначали комбинацию БАБ + диуретик. В отсутствие тахикардии и периферических отёков предполагали повышение системного сосудистого сопротивления (СС) и добавляли вазодилататоры.
Высокое системное СС в сочетании с нарушением функции почек может не проявляться периферическими отёками. В этом случае увеличивали дозировку диуретика в дополнение к вазодилататору или вместо него [16, 17].
S. Mann с соавторами разработали схожий алгоритм [18, 19]. Выбор дополнительного ЛС проводится в зависимости от их воздействия на прессорные механизмы: повышение объёма циркулирующей крови (ОЦК), стимуляция ренин-ангиотензин-альдостероновой системы (РААС) или симпатической нервной системы.
Предполагается, что пациент уже получает терапию ЛС, одно из которых снижает ОЦК (диуретик), а другое блокирует РААС (такие препараты, как ИАПФ, БРА, БАБ или прямой ингибитор ренина).
Повышение эффективности фармакотерапии достигается одной из тактик:
- понижение ОЦК путём добавления диуретика часто в совокупности с АМР;
- уменьшение симпатической активности путём комбинированной альфа+бета-блокады.
Схему лечения выбирают исходя из клинической симптоматики:
- при перегрузке объёмом (чрезмерное употребление соли, отёчный синдром) добавляли АМР (спиронолактон);
- при увеличении симпатической активности (синусовая тахикардия, включая пациентов с синдромом обструктивного апноэ во сне, алкоголизмом, лабильной АГ) дополняли лечение a-адреноблокатором или БАБ.
В результате у 89 % пациентов удалось достичь целевого уровня АД. Из них у 54 % проводилось усиление диуреза, у 25 % к схеме лечения присоединён aльфа-адреноблокатор, у 21 % применялись обе стратегии в комбинации. В качестве дополнительных антигипертензивных ЛС чаще назначались АМР (67 %) и доксазозин (37,5 %).
Активность ренина как маркер для терапии артериальной гипертензии
Одним из маркеров для выбора терапии АГ является активность ренина плазмы. Попытки деления АГ на «низкорениновую» и «высокорениновую» проводились ещё в 80‑е гг. прошлого столетия.
Некоторые исследователи до сих пор пользуются классификацией B. Egan и соавторов [20], в которой пациентов с активностью ренина <0,65 нг/мл/ч относят к «объем-зависимым». У таких больных оправдано применение диуретиков, спиронолактона, АК или aльфа-адреноблокаторов.
Пациентов с активностью ренина >0,65 нг/мл/ч относят к «резистивным». Им показаны вазодилатирующие ЛС: ИАПФ, БРА, БАБ.
C. Furberg [21] считает, что если активность ренина <0,65 нг/мл/ч, то можно думать об отсутствии полной блокады РААС. При этом нужно отменить вазодилататоры. Для достижения целевого уровня АД возможно назначение второго диуретика.
При активности ренина >6,5 нг/мл/ч можно предполагать чрезмерную дегидратацию пациента. В этом случае отменяют диуретик. Для достижения целевых значений АД к терапии добавляют второй вазодилататор.
Активность ренина 0,65–6,5 нг/мл/ч говорит о полной блокаде РААС. Для достижения контроля АД назначают второй диуретик. При нормализации АД можно попытаться отменить вазодилататор.
Большинство перечисленных исследований направлено на создание схем комбинированной фармакотерапии АГ. Не во все из них были включены пациенты с РАГ.
Задержка жидкости и гиперпродукция катехоламинов — это одни из основных причин появления и поддержания резистентности к лечению у пациентов с АГ [18]. F. Finnerty ещё в 1971 высказал идею, до сих пор сохранившую свою актуальность: «Увеличение дозы антигипертензивных средств при избыточном объёме внеклеточной жидкости не влияет на АД».
В ряде исследований [14, 22] было продемонстрировано, что у пациентов с устойчивой АГ на фоне ХБП добавление или повышение дозы тиазидных или петлевых диуретиков вело к понижению систолического АД на 20–35 мм рт. ст.
Чрезмерная задержка жидкости может быть обусловлена приёмом вазодилататоров и повышением уровня альдостерона, что характерно для пациентов с РАГ [23–27].
Результаты исследований PHARES, ASPIRANT и PATHWAY-2
Отсутствие или недостаточная доза диуретиков в схеме лечения АГ является одной из главных причин низкой эффективности терапии. Усиление диуретической терапии (в том числе с использованием АМР) для лечения РАГ отражено в таких исследованиях, как PHARES, ASPIRANT и PATHWAY-2.
В исследовании PHARES был выполнен сравнительный анализ двух лечебных режимов:
- Последовательная блокада нефрона.
- Последовательная блокада РААС.
Объектом исследования стали пациенты с РАГ, получающие базовую терапию (ирбесартан 300 мг + гидрохлортиазид 12,5 мг + амлодипин 5 мг) и не достигшие целевого уровня АД.
Тактика блокады нефрона представляла собой дополнительное назначение спиронолактона 25 мг с дальнейшим усилением фуросемидом (20–40 мг) и амилоридом (5 мг).
Тактика последовательной блокады РААС включала дополнительное назначение рамиприла (5–10 мг) и бисопролола (5–10 мг). Более существенное понижение АД отмечалось у пациентов на 1 режиме терапии [28].
В исследовании ASPIRAN проводился анализ эффективности спиронолактона в терапии РАГ. Было выделено 2 группы пациентов:
- в дополнение к базисной терапии блокатором РАС, антагонистами кальция и тиазидными диуретиками назначали спиронолактон;
- базисная терапия + плацебо.
Через 8 недель в 1 группе отмечалось более существенное снижение уровня АД (на 10,5/3,5 мм рт. ст.) [29].
Исследование PATHWAY-2 было посвящено выбору дополнительного ЛС для лечения РАГ. Его объектом стали пациенты с АД ≥ 140 мм рт. ст. Базовая терапия включала максимально переносимые дозы ИАПФ/БРА+АК+диуретик.
В ходе исследования к комбинированной терапии поочерёдно (на 12 недель) добавляли одно из ЛС: спиронолактон, бисопролол, доксазозин и бисопролол. Лечение спиронолактоном показало более значимое понижение АД в сравнении с плацебо, доксазозином и бисопрололом. Наилучшие результаты терапии спиронолактоном отмечались в группе с низкой активностью ренина [30, 31].
Выводы
Авторы работы приходят к выводам, что не существует единых рекомендаций в отношении комбинированной терапии пациентов с РАГ. Подбор ЛС четвертой-пятой линий чаще всего проводится эмпирически на основании собственного клинического опыта.
На сегодняшний день наибольшую доказательную базу имеет добавление к стандартной трехкомпонентной терапии препаратов из группы антагонистов минералокортикоидных рецепторов. Остальные тактики лечения менее изучены.
Одна из важнейших задач современной кардиологии — это определение предикторов эффективности разных схем антигипертензивной терапии, что поможет разработать персонифицированный подход к терапии пациентов с РАГ.
23 июля 2023
Текст: Светлана Маляева
Фото: istockphotos.com/Ocskaymark
Выпуск: №235, июль 20232848 просмотров
2848 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль 1.jpg)


зарегистрированным пользователям