Если весной течёт из носа: современные подходы в лечении ринита
О роли назальных глюкокортикостероидов (ГКС) в лечении поллинозов и аллергического ринита
Актуальность проблемы
Аллергический ринит (АР) отличается высокой распространённостью во всём мире (до 32 %) и в нашей стране (10–24 %) [1, 2, 4, 5, 9]. Это заболевание не является жизнеугрожающим состоянием, но значительно снижает качество жизни пациентов. АР часто сочетается с другими атопическими проявлениями [3, 4, 5, 9, 16].
Значение назальных ГКС в терапии АР
Назальные ГКС (НГКС) являются препаратами первой линии при среднетяжелой и тяжёлой форме АР, «золотым стандартом» лечения» [1, 3]. На наш взгляд, обзор имеющейся информации о назальных глюкокортикоидах будет полезен не только практикующим врачам, но и работникам первого стола, провизорам.
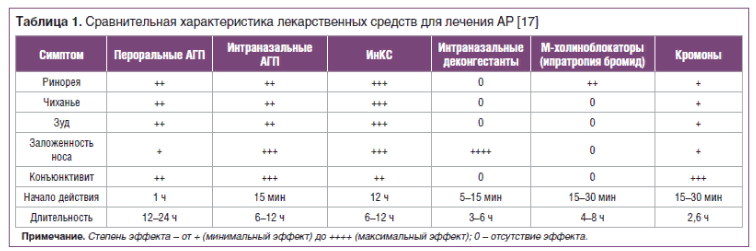
В таблице 1 приведены сравнительные характеристики разных групп препаратов для купирования основных проявлений аллергического ринита.
Назальные ГКС могут назначаться в качестве монотерапии и в сочетании с пероральными антигистаминными препаратами (АГП) [18, 7, 8]. При сравнительном анализе было установлено, что при продолжительной терапии НГКС имеют преимущество перед АГП [19, 7].
Научные исследования показали, что назальные ГКС затрагивают все звенья патогенеза АР [20, 21, 15], их лечебное воздействие связано с противовоспалительным и десенсибилизирующим эффектом. Преимуществом этой группы препаратов перед пероральными ГКС служит минимизация риска системного действия на организм [21, 22, 15].
Для назальных ГКС характерна высокая эффективность, быстрота наступления и продолжительность терапевтического воздействия, высокий профиль безопасности [21, 22, 23, 15].
Основные действующие вещества в группе НГКС и их свойства
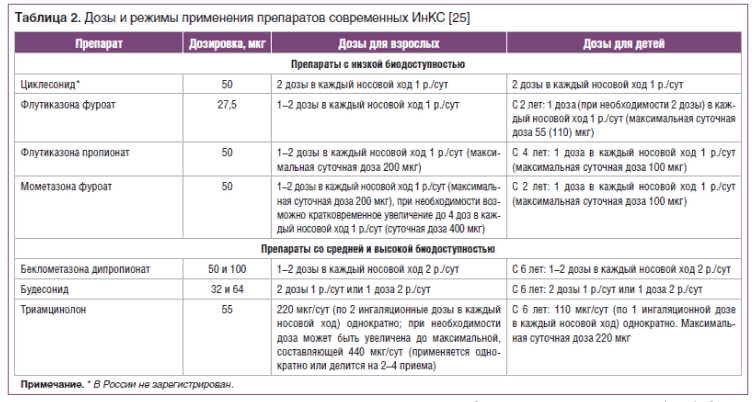
В настоящее время выбор этой группы препаратов достаточно широк. Основные действующие вещества: беклометазона дипропионат, будесонид, флутиказона фуроат, флутиказона пропионат, мометазона фуроат [24]. Дозировки и режимы их назначения приведены в таблице 2 [25].
При назначении назальных ГКС проводят комплексную оценку их основных свойств [26]:
- фармакодинамических (сродство к соответствующим рецепторам);
- физико-химических (липофильность);
- фармакокинетических (системная биодоступность).
От степени сродства к ГКС-рецепторам зависит сила действия лекарственного средства; от липофильности — степень и скорость его прохождения через мембраны клеток, достижение ГКС-рецептора, длительность нахождения на слизистой носовой полости; от системной биодоступности — частота развития побочных эффектов, лекарственная переносимость и приверженность к терапии [27].
При сравнении сродства к ГКС-рецепторам у назальных ГКС прослеживается уменьшение этого показателя по направлению от начала к концу последовательности:
ФФ (флутиказона фуроат) — МФ (мометазона фуроат) — ФП (флутиказона пропионат) — ТРИАМ (триамцинолон) — БУД (будесонид) — ДМ (дексаметазон) [28];
ФП (флутиказона пропионат) — МФ (мометазона фуроат) — БУД (будесонид) > ФЛУ (флунизолид, не зарегистрирован в России) — ТРИАМ (триамцинолон) [29].
Показатели липофильности и растворимости у назальных ГКС соответственно составляют: у МФ — 5,5 и <0,01, у ЦИК (циклесонид) — 5,0 и <0,01, у ФП — 3,89 и <0,01, у БДП (беклометазона дипропионат) — 4,59 и <0,01, у БУД — 2,32 и 16,0 [30].
Самая высокая липофильность отмечается у МФ, ФФ и ФП, что помогает лучшему проникновению и распределению в слизистой и пазухах носа [30]. Эти средства депонируются в тканях, их постепенное высвобождение ведёт к росту продолжительности действия, что даёт возможность использовать данные средства один раз в сутки [4].
Начальный эффект назальных ГКС проявляется в 1–3 сутки лечения, максимальный — отмечается спустя несколько дней [31]. Разные НГКС имеют разные сроки начального проявления клинического эффекта: мометазона фуроат — 5–7 ч.; флутиказона фуроат — 8 ч.; циклесонид — 10 ч.; флутиказона пропионат, будесонид — 12–24 ч.; триамцинолон — 24 ч.; беклометазона дипропионат — 72 ч. [32].
Клиническая эффективность НГКС
За клиническую эффективность и безопасность НГКС отвечают следующие показатели:
- депозиция (коррелирует с вязкостью, жидкость с низкой вязкостью распределяется до 99 %);
- абсорбция (обусловлена липофильностью и величиной частиц);
- клиренс (между скоростью выведения и вязкостью отмечается обратная зависимость: жидкость с низкой вязкостью быстрее выводится) [26].
Таким образом, идеальным считается интраназальный спрей с суспензией, обладающей одновременно высокой депозицией и вязкостью. Это противоречие преодолимо тиксотропностью НГКС — обратимым снижением вязкости при механическом встряхивании (Па˙с) [26, 33].
Резюмируя, наилучший аппликационный эффект в носовой полости достигается высокой начальной и конечной вязкостью [33]. Это качество лучше выражено у мометазона фуроата: 58,6 (Па˙с), а у беклометазона дипропионата этот параметр равен всего 3,5 (Па˙с) [26].
Из всех назальных ГКС самую низкую биодоступность (менее 0,1 %) имеет мометазона фуроат [34, 35]. Это обеспечивает невысокий риск развития осложнений при его использовании. Диапазон системной биодоступности других НГКС варьирует от <2 % у флутиказона пропионата до 10 % у будесонида, от 44 % у беклометазона до >80 % у дексаметазона [34, 35].
По итогам системного метаанализа мометазона фуроат имеет высокий профиль безопасности, не провоцирует развитие побочных реакций, свойственных пероральным ГКС, не тормозит работу коры надпочечников, не замедляет рост у детей, безопасен при использовании в период вынашивания ребёнка [35]. Продолжительное применение не приводит к атрофии слизистой носа и пазух [35].
Геномный механизм состоит в комплиментарном сцеплении ГКС с соответствующими рецепторами в клеточной цитоплазме. Образованный комплекс поступает в ядро, где он стимулирует экспрессию генов, обеспечивающих образование противовоспалительных антигенов [14, 29–32].
Внегеномный механизм заключается в прямом подавлении комплексами «ГКС — ГКС-рецептор» факторов транскрипции провоспалительных антигенов [28].
Из-за того, что у мометазона фуроата превалирует внегеномный механизм, реализация противовоспалительного эффекта происходит раньше, чем у прочих ГКС, с минимальным действием на геном, что обеспечивает его высокий уровень безопасности [35].
Оценка эффективности НГКС
Несмотря на внедрение новых лекарственных средств, долго не было метода, позволяющего сравнить эффективность использования НГКС. Немецкие учёные предложили применять для этого терапевтический индекс (Therapeutic index — TIX) [4, 5, 6, 10].
Он вычисляется как соотношение суммарной эффективности, рассчитанной по трём основным показателям (соответственно общим баллам назальных и глазных проявлений, общей оценке пациентами) и суммарной безопасности ГКС, определённой по трём показателям (частоте развития эпистаксиса — кровотечений из носа, воздействию на содержание кортизола, побочным явлениям со стороны глаз — росту внутриглазного давления и появлению катаракты) [36, 6].
В таблице 3 продемонстрированы TIX, разработанные на базе обзора результатов 84 исследований, проведённых в отношении 6 действующих веществ [36].
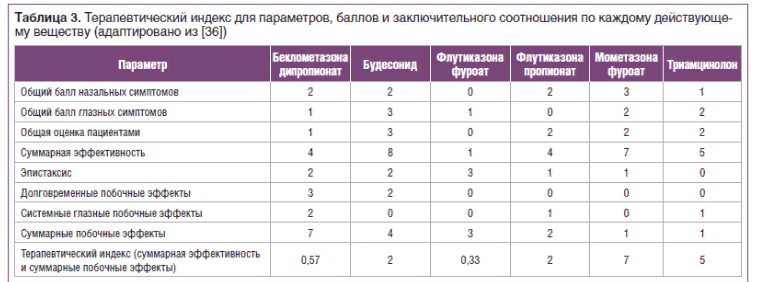
Все они показали высокую эффективность и безопасность. Самый высокий TIX отмечен у мометазона фуроата [36, 12, 17]. Многочисленные клинические испытания [35] показали его эффективность и безопасность при АР, остром и хроническом риносинусите, гипертрофии аденоидов и среднем отите у детей [37] с 2‑х летнего возраста [35]. Безопасность подтверждена не только научно-исследовательским путём, но и в результате практического применения мометазона фуроата >20 лет [11, 33, 17].
Рекомендуемая доза при аллергическом рините — 50 мкг в каждый носовой ход однократно в течение 1–6 месяцев и больше [35, 17]. Она позволяет купировать проявления заболевания на сутки.
Заключение
Назальные ГКС рекомендуют в терапии АР как препараты первой линии. Они просты в применении, эффективны и безопасны. Такое сочетание способствует повышению приверженности пациентов к лечению [4, 5, 12].
Клинические исследования и практический опыт применения подтверждают высокую эффективность и безопасность мометазона фуроата. Об этом говорят объективные показатели и субъективное мнение самих пациентов [4, 5, 12].
18 марта 2024
Текст: Светлана Маляева
Фото: www.istockphoto.com/marketlan
Выпуск: №243, март 20246556 просмотров
6556 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль


зарегистрированным пользователям