Боль и кахексия
Пожилой мужчина обратился за помощью в связи с резкой болью в конечностях
По материалам: Diabetic neuropathic cachexia: a case reportDeeb D Naccache, William B Nseir, Moshe Z Herskovitz and Mogher H KhamaisiJournal of Medical Case Reports 2014, 8:20
Источник: www.jmedicalcasereports.com/content/8/1/20
В поликлинику обратился 71‑летний мужчина с жалобами на резкую боль в верхних и нижних конечностях и в области ягодиц, беспокоящую его уже три месяца. Из анамнеза известно, что мужчина в течение 29 лет страдает сахарным диабетом, осложненным диабетической нефропатией и нейропатией. По визуальной аналоговой шкале (visual analog scale, VAS) выраженность боли была оценена на 10 баллов из 10. Кроме того, пациент отметил, что похудел на 20 кг, жаловался на полное отсутствие аппетита, нервозность, подавленное настроение и апатию, бессонницу, тремор, запоры, а также головокружения и слабость при резкой смене положения тела. При этом прием гипотензивных препаратов был сведен к минимуму некоторое время назад — рамиприл отменен, а доза атенолола снижена.
Из данных клинико-лабораторных тестов, проведенных ранее, — показатель гликированного гемоглобина (HbА1с) на дозе 30 ЕД/сут смешанного инсулина и 850 мг трижды в день метформина составлял 9,1 %. Кроме того, обращали ни себя внимание высокая концентрация ферритина, низкий уровень сывороточного железа (таблица 2), анемия средней степени тяжести и умеренно выраженная хроническая почечная недостаточность (таблица 1).
Известно, что за несколько недель до визита в поликлинику пациент прошел эндоскопическое обследование желудочно-кишечного тракта и полное КТ-сканирование с целью обнаружения неопластического процесса. Однако кроме лимфангиэктазии и артериовенозной мальформации в тонкой кишке и узлового зоба других патологических изменений обнаружено не было.Объективный статус при обращении — эмоциональный фон подавленный. Кожные покровы бледные, АД 124/63 мм. рт. ст., пульс — 107 уд/мин, вес — 86,9 кг, рост — 171 см, ИМТ — 29,7 кг/м2. Черты лица грубые с утолщенными губами и широкими ноздрями; утолщенные фаланги пальцев рук. Отмечается мелкая дрожь в ладонях. Сухожильные рефлексы с верхних и нижних конечностей снижены, гипестезия рук и стоп по типу «перчаток» и «носков», мышечная сила снижена в дистальных отделах верхних конечностей.
Из истории болезни — у пациента артериальная гипертензия, снижение слуха, синдром карпального канала в правой руке, синдром обструктивного апноэ во сне, гиперлипидемия, грыжа пищеводного отверстия диафрагмы и рефлюкс-эзофагит, доброкачественная гиперплазия предстательной железы.
Узловой зоб размером 3,3 см в диаметре был подтвержден данными УЗИ. За месяц до проведения КТ с йод-содержащим контрастом уровень ТТГ был 0,19 мЕД/мл (при норме 0,35–4,94 мЕД/мл). Впоследствии продукция ТТГ оказалась подавленной, а уровень тиреоидных гормонов, наоборот, был повышенным (таблица 1). Сцинтиграфия щитовидной железы выявила асимметричный зоб и слабое поглощение изотопа технеция. Поглощение радиоактивного йода щитовидной железой было в пределах нормы — 1 % и 10 % через 2 часа и 24 часа соответственно. Тонкоигольная аспирационная биопсия выявила клетки фолликулярного эпителия в узле.
Данные лабораторных анализов: ОАК без особенностей; функции печени и почек без выраженных изменений; тестостерон, пролактин, ФСГ, ЛГ, В12, СРБ в пределах нормы. Иммунологические тесты не выявили ревматической патологии. ВИЧ — отрицательный.
Лечащие врачи предположили, что выраженная нейропатия, в основе которой лежат катаболический и воспалительный механизмы, может быть причиной сильного истощения организма, потери массы тела, анемии и изменения показателей острофазового воспалительного ответа (ферритина и свободного железа). В дальнейшем концентрация ферритина за время проводимого лечения заметно снизилась, однако свободное железо еще длительное время оставалось на низком уровне (таблица 2).
Электрофизиологические тесты выявили сенсомоторную аксональную полинейропатию.Уровень СТГ и инсулин-подобного фактора роста-1 (ИФР-1) свидетельствовал об акромегалии у пациента (таблица 1). Проведенное МРТ-исследование головного мозга с контрастным усилением (с гадолинием) выявило опухолевидное образование в области гипофиза размером 3×5×3 мм.
Подавленное настроение было связано главным образом с выраженной нейропатической болью. Снижение массы тела почти на 20 % за столь короткий срок указывало на развитие у пациента редко встречающейся диабетической нейропатической кахексии.
Для этого типа кахексии характерны такие проявления, как катастрофическое снижение массы тела, анорексия, ортостатическая гипотензия, изменение настроения и нарушения сна.
Первостепенной задачей для лечащих врачей стало снижение выраженности нейропатической боли, на втором месте по значимости симптомов — нормализация уровня гормонов щитовидной железы, и, наконец, третьей задачей было проведение соответствующего лечения акромегалии.
Для лечения нейропатии был назначен прегабалин (алкилированный аналог гамма-аминомасляной кислоты), относящийся к группе противоэпилептических препаратов.
Кахексия может быть установлена в следующих случаях:
-низкая масса тела (менее 70 % от идеальной) или индекс массы тела (ИМТ) менее 16–17 кг/м2;
-документированное резкое снижение массы тела более чем на 7,5–10 % от исходной.
Таким образом, в диагностике кахексии важно учитывать не только низкие весовые показатели, но и скорость снижения массы тела.
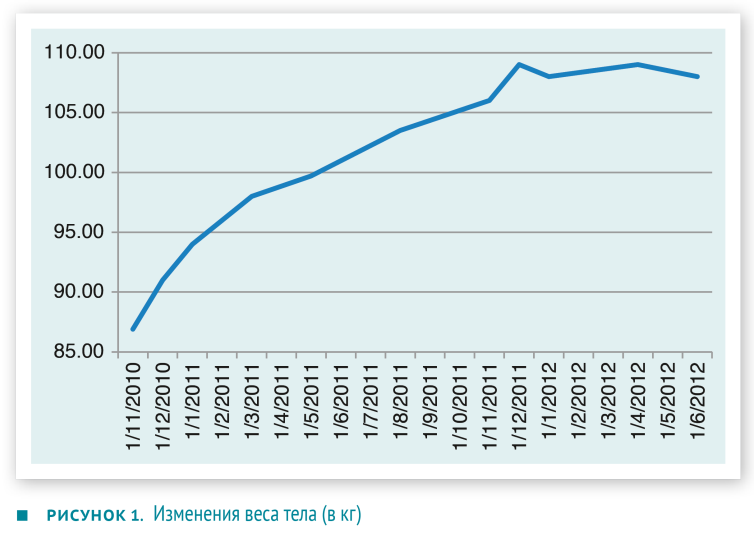
Доза 75 мг в сутки, установленная с учетом клиренса креатинина, позволила добиться положительного эффекта. По шкале VAS выраженность боли снизилась до 4–5 баллов. У пациента появился аппетит, он стал прибавлять в весе (рисунок 1). Однако иногда после приема пищи возникала рвота. Сцинтиграфия опорожнения желудка — минимальное прохождение пищи, меченной радиоизотопом, в тонкую кишку наблюдалось через 3,5 часа с момента приема пищи, что указывало на гастропарез.Для того чтобы удерживать стабильный уровень гликемии, доза смешанного инсулина была увеличена до 70 ЕД/сут. Спустя три месяца уровень HbА1с снизился до 7,5 %, пациенту назначили пероральные гипогликемические препараты — метформин и вилдаглиптин. Развившееся вскоре состояние гипогликемии заставило снизить дозу инсулина и перейти от смешанного инсулина к терапии базальным инсулином (28 ЕД/сут).
Интересно отметить, что через 8 недель произошло спонтанное восстановление показателей функции щитовидной железы до нормальных значений. Уровень ТТГ вернулся к исходному значению через 16 недель.
Данные МРТ и гормонального статуса (таблица 1) указывали на то, что акромегалия у пациента была вызвана аденомой гипофиза. Пациент отказался от проведения аденомэктомии и предпочел медикаментозное лечение синтетическими аналогами соматостатина. Однако прием ланреотида (60 мг/мес) в течение нескольких месяцев не позволил нормализовать уровень ИФР-1 (437 нг/мл). Кроме того, отмечались побочные эффекты — колебания уровня глюкозы и учащение приступов рвоты после приема пищи. Повышение гликемии предположительно было связано с ятрогенным влиянием на регуляцию гомеостаза глюкозы (за счет подавления эндогенной продукции инсулина). В связи с этим пациенту было рекомендовано хирургическое лечение аденомы гипофиза.
Обсуждение
Несмотря на значительную потерю веса, ведущим клиническим симптомом являлась выраженная нейропатическая боль, что и определило тактику лечения.
В данном случае боль выступает в качестве этиологического фактора, а не следствия потери массы тела, обусловленной сдвигом баланса обмена веществ в сторону катаболических процессов.
Гипертироксинемия, обнаруженная у пациента, была достаточно быстро скорригирована. Лечение гипергликемии потребовало больших усилий с многократными ежедневными инъекциями инсулина. Максимальная доза инсулина (70 ЕД/сут), которую получал пациент на пике нейропатической боли, была намного выше той дозы инсулина (28 ЕД/сут), которая позволяла позднее поддерживать гликированный гемоглобин на уровне 7,2 %. Такое снижение дозы инсулина отражало ослабление влияния боли на катаболические процессы в организме.
Диабетическая нейропатическая кахексия определяет состояние общего истощения организма с потерей мышечной массы и жира [1–3]. Повышенный уровень ферритина является маркером острофазного ответа [4]. Несмотря на очевидные различия, нейропатическая боль по сценарию развития патологического процесса схожа с болевым синдромом при хирургическом стресс-ответе.
Нарушения, наблюдаемые при хирургическом стресс-ответе, крайне типичны и для кахексии: дистресс, глюконеогенез из свободных жирных кислот, а также повышенные процессы распада белков в организме [5]. Сывороточное железо — это негативный реактант острой фазы воспаления [4], т. е. его концентрация понижается при воспалительной реакции. Снижение ферритина в плазме крови, наблюдаемое при лечении пациента, отражало уменьшение воспалительного процесса, сопровождающего диабетическую кахексию. Однако уровень железа оставался низким (таблица 2).
Нарастание массы тела можно было объяснить значительным замедлением процессов метаболического распада, а также снижением уровня гликемии.
Чем меньше уровень катаболизма в организме, тем меньше эндогенная продукция глюкозы. Снижение выраженности нейропатической боли и интенсивная инсулинотерапия — направлены на анаболические процессы, что в конечном итоге позволило восстановить вес пациента. Подобный случай уже был описан в литературе [3].
Акромегалия может напрямую способствовать развитию и прогрессированию периферической нейропатии. С другой стороны, избыток СТГ может привести к возникновению сахарного диабета, который в свою очередь инициирует развитие периферической нейропатии. В связке акромегалия-диабет-нейропатия очень сложно определить, какое из состояний является этиологическим, а какое способствует развитию нейропатии. В литературе нет данных о том, что акромегалия в активной фазе ведет к сдвигу обмена веществ в сторону катаболизма. С другой стороны, приведенный клинический случай служит примером того, что несвязанные между собой на первый взгляд синдромы (артериальная гипертензия, апноэ во сне, синдром карпального канала) могут иметь общую причину — акромегалию.
Заключение
Описываемый клинический пример демонстрирует необходимость раннего начала лечения нейропатической боли и сдерживания катаболических процессов, сопровождающих боль.
Случай диабетической нейропатической кахексии, с которым столкнулись врачи, иллюстрирует тактику ведения пациента с широким спектром клинических симптомов, в частности со значительной потерей веса, выраженной нейропатической болью, неконтролируемым диабетом, ятрогенным поражением щитовидной железы, недиагностированной акромегалией. Кроме того, пример демонстрирует, как лечение акромегалии ланреотидом может обострить течение сопутствующей патологии.
Диабетическая нейропатическая кахексия аналогична острофазному ответу при катаболическом истощении организма. Однако авторы статьи рассчитывают на хороший прогноз в терапии диабетической нейропатической кахексии у пациента, поскольку сумели вовремя определиться с диагнозом и начать лечение.
Публикация клинического случая и сопутствующих иллюстраций осуществлялись с одобрения больного. Копия подписанного информированного согласия находится у главного редактора журнала Journal of medical case reports.
6038 просмотров
Поделиться ссылкой с друзьями ВКонтакте Одноклассники
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.

 Катрен Стиль
Катрен Стиль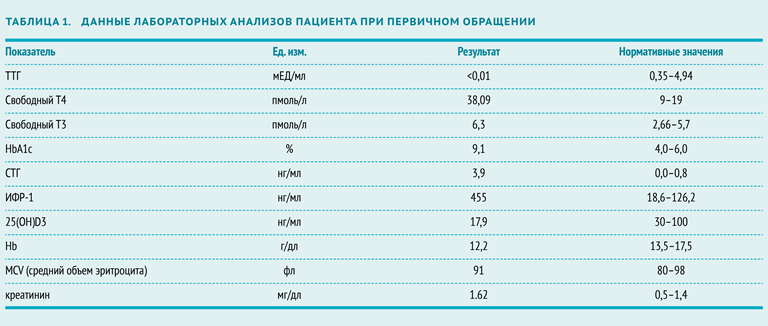


зарегистрированным пользователям